por Kiko Ramos | May 29, 2025 | Análisis de equipos
La regulación de dispositivos médicos es un pilar esencial para garantizar la seguridad del paciente, la eficacia médica y la calidad del diagnóstico en todo el sistema sanitario. Todos los productos sanitarios deben cumplir con exigentes requisitos legales y técnicos antes de ser comercializados y utilizados en la práctica clínica.
En este contexto, la aplicación de diferentes medidas y normativas para la regulación de equipos médicos tiene el objetivo de proteger a los usuarios. Y, al mismo tiempo, aportar confianza a los profesionales sanitarios, transparencia a los procesos de fabricación y trazabilidad en toda la cadena de suministro.
No obstante, es necesario destacar que certificar un equipamiento médico no es un trámite administrativo más. Se trata de un proceso multidisciplinar que abarca desde el diseño y la validación clínica hasta la implementación de sistemas de calidad, la gestión de riesgos y la vigilancia postcomercialización.
Pero, ¿cuáles son las diferentes normativas y procesos que se deben aplicar para comercializar y utilizar dispositivos médicos en la práctica clínica? En el siguiente artículo, realizamos una guía completa sobre la regulación de equipamientos médicos y los marcos legales actuales, tanto a nivel nacional y europeo como internacional.
¿Qué son los dispositivos médicos?
Los equipos médicos son dispositivos, aparatos o sistemas que se utilizan en la prevención, diagnóstico, tratamiento o rehabilitación de enfermedades y condiciones médicas. Abarcan desde productos sanitarios sencillos como jeringuillas o termómetros hasta tecnologías complejas como equipos de resonancia magnética, ecógrafos, sistemas de monitorización remota o software IA de radiodiagnóstico basado en la inteligencia artificial.
Los dispositivos médicos pueden clasificarse en distintas categorías según su nivel de riesgo para el paciente y el usuario, lo que influye directamente en el tipo de regulación y certificación que deben cumplir.
Regulación de dispositivos médicos: Las diferentes normativas y procesos
La regulación de los dispositivos médicos varía según el país o la región, pero en general, todos los marcos normativos comparten un objetivo común: asegurar que los productos sean seguros y eficaces para su uso clínico. A continuación, repasamos las diferentes normativas y procesos:
El marcado CE en el contexto europeo
Para lanzar un producto sanitario o un equipamiento médico al mercado y poder comercializarse en la Unión Europea, se debe disponer de marcado CE. El marcado CE es el requisito legal que autoriza la comercialización de un dispositivo médico en la Unión Europea (UE) y el Espacio Económico Europeo (EEE).
Indica que el producto cumple con las disposiciones del Reglamento (UE) 2017/745 sobre productos sanitarios, la denominada normativa MDR, y puede circular libremente dentro del mercado europeo. Este reglamento empezó a utilizarse en 2017 y sustituyó a la anterior Directiva 93/42/CEE con el objetivo de reforzar la seguridad, la trazabilidad y el control postcomercialización de los dispositivos.
El primer paso para determinar el proceso de marcado CE es realizar la clasificación de los equipos médicos según su riesgo. En función del tipo de riesgo, la normativa MDR define un nivel de documentación técnica y un proceso regulatorio para garantizar el acceso al mercado europeo. En concreto, los productos sanitarios se dividen en cuatro clases:
- Clase I: Riesgo bajo
- Clase IIa: Riesgo moderado
- Clase IIb: Riesgo elevado
- Clase III: Riesgo muy elevado. Uso de dispositivos implantables/invasivos críticos
¿Qué implica el marcado CE?
El marcado CE no es un sello de calidad, sino un indicador de conformidad legal a nivel europeo. Garantiza que el fabricante ha seguido una serie de procesos que certifican que la seguridad y la eficacia del dispostivo médico:
- Evaluación del dispositivo conforme a los requisitos legales de la normativa MDR.
- El uso del dispositivo médico es seguro y eficaz cuando se utiliza según las instrucciones.
- Implementación de un sistema de gestión de calidad adecuado.
- Uso de mecanismos de vigilancia postcomercialización y seguimiento clínico continuo.
- Evaluación mediante un Organismo Notificado.
FDA Approval en Estados Unidos
En Estados Unidos, la Food and Drug Administration (FDA) es la agencia gubernamental responsable de la regulación, supervisión y autorización de la comercialización de los dispositivos médicos.
Se desarrolla a través del Center for Devices and Radiological Health (CDRH), entidad que garantiza que todos los dispositivos médicos sean seguros, eficaces y fabricados conforme a estándares de calidad antes de llegar al mercado. Clasifica los productos en tres categorías:
- Clase I: Bajo riesgo, sujetos a controles generales.
- Clase II: Riesgo moderado, requieren una presentación 510(k) para demostrar que son sustancialmente equivalentes a otro dispositivo legalmente comercializado.
- Clase III: Riesgo alto. Requieren aprobación previa a la comercialización (PMA) con evidencia clínica detallada.
Diferencias clave entre FDA Approval y marcado CE
| Aspecto |
FDA (EE. UU.) |
CE (UE) |
| Ámbito |
Estados Unidos y países que reconocen la FDA |
Unión Europea y países que aceptan el marcado CE |
| Objetivo |
Autorizar la comercialización de los equipos médicos bajo la supervisión directa de la FDA |
Certificar que el producto cumple los requisitos de seguridad y rendimiento definidos en el Reglamento MDR |
| Enfoque |
Evaluación previa a la comercialización más estricta |
Evaluación basada en conformidad del fabricante |
| Revisión clínica |
PMA exige ensayos clínicos |
Solo Clase III requiere evidencia clínica robusta |
| Tiempos |
Largos, especialmente en PMA |
Más ágiles en las clases I y IIa |
| Organismo evaluador |
Agencia pública (FDA) |
Organismo Notificado independiente |
Regulación de dispositivos médicos en España: El papel de la AEMPS
En España, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) es el organismo responsable de aplicar la normativa nacional y europea sobre dispositivos médicos. Su misión principal es garantizar la calidad, seguridad, eficacia y correcta información de todos los productos sanitarios que se comercializan o utilizan en el país.
La AEMPS depende del Ministerio de Sanidad y actúa como autoridad competente para supervisar el cumplimiento del Reglamento (UE) 2017/745 sobre productos sanitarios (MDR), así como otras disposiciones nacionales. En España, el marco legal sobre la regulación de dispositivos médicos se articula en función de las siguientes normativas:
- Real Decreto 192/2023, por el que se regulan los productos sanitarios: Es la norma nacional más reciente y completa en materia de productos sanitarios. Su objetivo es adaptar el Reglamento (UE) 2017/745 al ordenamiento jurídico español.
- Ley 29/2006, de garantías y uso racional de los medicamentos y productos sanitarios: Esta Ley es el marco jurídico general para todo lo relacionado con medicamentos y productos sanitarios en España. Aunque nació centrada en fármacos, ha sido modificada y ampliada para incluir dispositivos médicos.
- Guías y procedimientos técnicos emitidos por la propia AEMPS: La AEMPS emite regularmente documentos técnicos, instrucciones y guías que ayudan a los fabricantes y agentes económicos a interpretar y cumplir correctamente las normas.
Las normas ISO: Estandarización y control de calidad en dispositivos médicos
Las normas ISO (International Organization for Standardization) son estándares internacionales voluntarios que establecen buenas prácticas para el diseño, producción, evaluación y gestión de productos y servicios.
En el ámbito de los dispositivos médicos, no sustituyen a la legislación, como la normativa MDR en el contexto europeo o la aprobación FDA en Estados Unidos. Sin embargo, son instrumentos clave para demostrar conformidad con los requisitos regulatorios y garantizar la seguridad, eficacia y trazabilidad del producto. A continuación, destacamos las normas ISO más relevantes:

ISO 13485:2016 – Sistemas de gestión de calidad para dispositivos médicos
Es la norma más importante en este sector. Establece los requisitos para un sistema de gestión de calidad (SGC) específicamente adaptado a fabricantes y distribuidores de dispositivos médicos.
Aplicación regulatoria
No es obligatoria por ley, pero la implantación de un sistema ISO 13485 facilita la obtención del marcado CE, ya que reduce errores y demuestra un compromiso con la calidad y la seguridad del paciente.
ISO 14971:2019 – Gestión de riesgos para dispositivos médicos
Establece un marco estructurado para identificar, evaluar, controlar y monitorizar los riesgos relacionados con un dispositivo médico a lo largo de su ciclo de vida.
Aplicación regulatoria
Es obligatoria en el contexto del MDR para demostrar que se ha realizado una evaluación de riesgos exhaustiva. Se integra estrechamente con la documentación técnica y la evaluación clínica del dispositivo.
ISO 10993 – Evaluación biológica de dispositivos médicos
Esta serie de normas aborda los ensayos biocompatibles necesarios para garantizar que los materiales en contacto con el cuerpo humano no sean tóxicos ni provoquen reacciones adversas.
Aplicación regulatoria
Estas pruebas son obligatorias para todos los dispositivos que entren en contacto directo o indirecto con el cuerpo humano. Su cumplimiento forma parte del expediente técnico que se presenta para el marcado CE o la aprobación FDA.
ISO 14155: Ensayos clínicos de dispositivos médicos en seres humanos – Buenas prácticas clínicas
Establece los principios y requisitos para el diseño, conducción, grabación y presentación de ensayos clínicos realizados en seres humanos con dispositivos médicos.
Aplicación regulatoria
Es obligatoria para fabricantes que realicen estudios clínicos previos a la certificación CE o FDA, especialmente para dispositivos de clase III o implantables.
ISO 62304: Software para dispositivos médicos – Procesos del ciclo de vida del software
Define los requisitos para el desarrollo, mantenimiento y soporte del software que se utiliza como parte de un dispositivo médico, o que constituye un Software as a Medical Device (SaMD).
Aplicación regulatoria
Resulta obligatoria para cualquier software sanitario que afecte al diagnóstico, tratamiento o monitorización de pacientes, ya sea independiente o integrado en hardware. Se trata de un aspecto clave en productos como apps médicas, sistemas PACS o ecógrafos inteligentes.
Conclusión
La seguridad del paciente empieza con una certificación responsable. Las aplicaciones regulatorias son un aspecto clave para lograr una comercialización segura y eficaz en el ámbito de los dispositivos médicos. Más allá de un mero requisito legal, representan un proceso estructurado y riguroso que garantiza que los productos sanitarios han sido diseñados, evaluados y fabricados bajo los más altos estándares de calidad, seguridad y eficacia.
Ya sea bajo el marco del marcado CE en Europa, la FDA en Estados Unidos o las autoridades sanitarias nacionales como la AEMPS en España, los procedimientos de evaluación y certificación son indispensables para asegurar que la innovación tecnológica en el sector salud llegue al mercado de forma responsable, eficiente y sostenible.
¿Necesitas un equipo médico? En ese caso, no dudes en contactar con nosotros y nuestro equipo de 4D te ayudará a elegir el mejor dispositivo médico en función de las necesidades de tu clínica u hospital.
Contacta con 4D
Kiko Ramos
CEO de 4D Médica. Experto en comercialización y distribución de equipamiento médico.

por Luis Daniel Fernádez | May 21, 2025 | Análisis de equipos
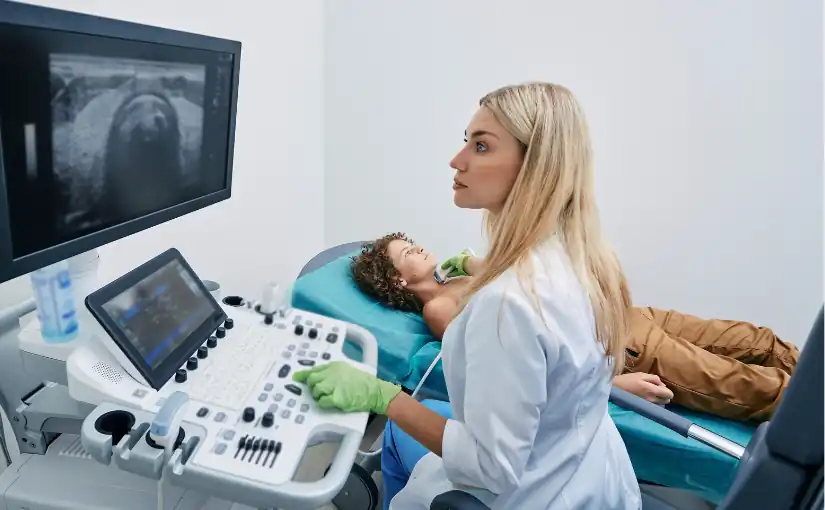
En la actualidad, el ecógrafo se ha consolidado como una herramienta fundamental en el área de diagnóstico por imágenes. Este dispositivo utiliza la tecnología de ultrasonido para obtener imágenes precisas y en tiempo real de las estructuras internas del cuerpo humano, facilitando la evaluación de órganos, tejidos y vasos sanguíneos sin necesidad de procedimientos invasivos.
La capacidad del ecógrafo para ofrecer información detallada, segura y rápida ha revolucionado la práctica clínica. El empleo de este equipo médico permite que los profesionales de la salud puedan detectar y monitorizar una amplia variedad de patologías de manera precoz y eficaz. Además, su versatilidad y portabilidad ha ampliado su uso a múltiples especialidades médicas.
El uso del ecógrafo se emplea para realizar ecografías con el objetivo de analizar los órganos y tejidos de forma interna. Se trata de una de las técnicas médicas más utilizadas, ya que destaca por ser un método rápido, eficaz y no invasivo. Se utiliza, principalmente, para detectar enfermedades y anomalías, monitorizar la salud de los pacientes, estudiar el desarrollo y crecimiento del bebé durante el embarazo, así como para guiar ciertos procedimientos médicos.
A diferencia de otras técnicas de imagen, como los rayos X o la Tomografía Axial Computarizada (TAC), el ultrasonido no utiliza radiación ionizante, lo que lo convierte en una técnica más segura. Además, su portabilidad y facilidad de uso ha permitido su integración en consultas, urgencias y unidades de cuidados intensivos, facilitando la toma de decisiones clínicas en tiempo real y mejorando la atención al paciente.
En el siguiente artículo, analizamos el origen de este equipo médico hasta la actualidad, cómo funciona un ecógrafo, así como sus aplicaciones en la práctica clínica.
Origen del ecógrafo: Desde sus inicios hasta la actualidad
El desarrollo del ecógrafo está estrechamente ligado al desarrollo de la tecnología del ultrasonido y su aplicación en el ámbito médico.

Primeros estudios: Descubrimiento del efecto piezoeléctrico
Los primeros estudios sobre ondas ultrasónicas datan de finales del siglo XIX, cuando los físicos franceses Pierre y Jacques Curie descubrieron en 1880 el efecto piezoeléctrico. Este fenómeno físico consiste en la capacidad de ciertos materiales, como el cuarzo y algunos cristales cerámicos, para generar una carga eléctrica cuando se someten a una presión mecánica.
La importancia del efecto piezoeléctrico en la ecografía es fundamental, ya que constituye la base del funcionamiento del transductor o sonda del ecógrafo. En la práctica, los cristales piezoeléctricos ubicados en el transductor convierten las señales eléctricas en vibraciones ultrasónicas (ondas de ultrasonido), que se transmiten al cuerpo del paciente. Mediante el efecto piezoeléctrico, estos ecos se transforman en señales eléctricas que el ecógrafo procesa para generar imágenes en tiempo real.
Desarrollo del primer ecógrafo: Del efecto piezoeléctrico y los ultrasonidos al campo médico
Tras el descubrimiento del efecto piezoeléctrico, el fenómeno se aplicó de forma inicial en campos industriales y militares, especialmente en el desarrollo de dispositivos de sonar para la detección submarina durante la Primera y la Segunda Guerra Mundial.
Sin embargo, el potencial de los ultrasonidos y el efecto piezoeléctrico para generar y recibir ondas acústicas no pasó desapercibido para la comunidad científica y médica. La adaptación de esta tecnología al ámbito médico comenzó a mediados del siglo XX. El médico escocés Ian Donald, junto con el ingeniero Tom Brown, fueron los investigadores pioneros que comenzaron a aplicar el efecto piezoeléctrico en la exploración clínica, asentando las bases de la ecografía médica.
Concretamente, fue en la década de 1950, cuando los investigadores desarrollaron el primer prototipo de ecógrafo clínico. Inicialmente, el ecógrafo se empleó en la obstetricia para la visualización del feto y la detección de patologías durante el embarazo, lo que supuso una revolución en el seguimiento prenatal.
De los años 60 y 70 hasta la actualidad: Avances en la ecografía
Durante los años 60 y 70, la tecnología del ultrasonido experimentó avances significativos. Se pasó de imágenes estáticas a ecografías en tiempo real, lo que permitió observar el movimiento de órganos y estructuras internas. Posteriormente, la incorporación del efecto Doppler posibilitó el estudio del flujo sanguíneo y la evaluación vascular, ampliando aún más las aplicaciones clínicas del ecógrafo.
En las últimas décadas, el desarrollo de la tecnología y la informática ha posibilitado la aparición de ecógrafos más compactos, portátiles y con una mayor resolución de imagen. Actualmente, el ecógrafo es una herramienta segura, eficaz y versátil que se utiliza en una amplia variedad de especialidades, desde la medicina de urgencias hasta la cardiología, la ginecología y la medicina interna. Por ello, se ha convertido en un equipo médico indispensable en la práctica médica.
Los ecógrafos de última generación: Innovación, tecnología e inteligencia artificial
En los últimos años, la tecnología ha avanzado mucho en el campo de la medicina. Los ecógrafos de última generación ofrecen imágenes en tecnología 3D, 4D y 5D, por lo que permiten visualizar el interior del cuerpo humano en movimiento y en tiempo real.
Una de las innovaciones más recientes son los ecógrafos que incorporan sistemas de procesamiento digital que aplican la inteligencia artificial en el análisis de imágenes médicas. El empleo de un software IA en equipos de ecografía proporciona una mayor rapidez, eficiencia, seguridad y precisión diagnóstica, proporcionando un análisis avanzado y detallado que mejora la toma de decisiones clínicas.
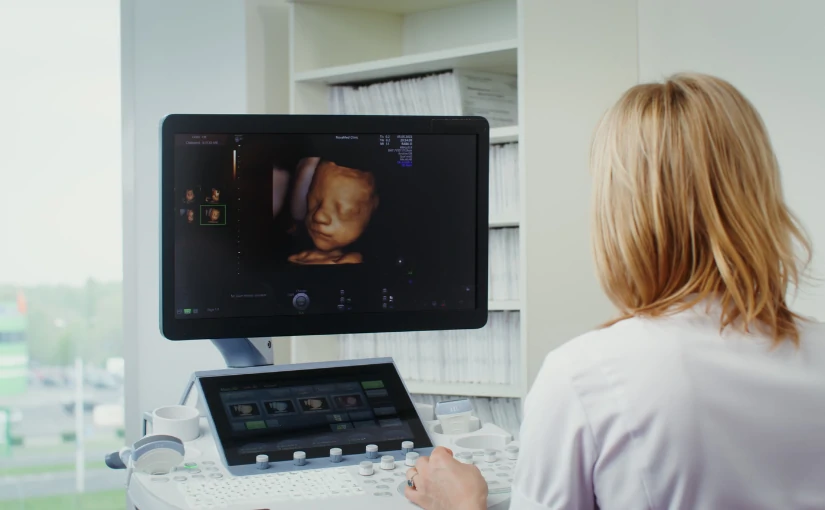
En este ámbito, destaca el uso de ecógrafos de última generación para visualizar el feto en tiempo real. Se conoce como ecografía emocional y permite que los padres puedan conocer al bebé antes de que nazca. Este tipo de ecografía combinan la tecnología 3D, que proporciona imágenes tridimensionales, con la tecnología 4D y 5D, que incorporan el movimiento en tiempo real con una elevada nitidez y calidad de imágenes. Con ello, se pueden ver los principales movimientos del bebé. Desde cómo bosteza, abre los ojos y se mueve hasta cómo cambia de posición.
Cómo funciona un ecógrafo: Procedimiento paso a paso
Los ecógrafos son una herramienta esencial en la práctica médica. Comprender su funcionamiento y el flujo de trabajo durante una ecografía es fundamental para garantizar la calidad diagnóstica y la seguridad del paciente. A continuación, abordamos cómo funciona un ecógrafo y el procedimiento que se realiza paso a paso:

1. Preparación del paciente y aplicación del gel conductor
En primer lugar, se indica al paciente la posición en la que se debe colocar según la zona a explorar y el tipo de diagnóstico a realizar. Antes de iniciar la exploración, se aplica el gel conductor sobre la piel del paciente. Tiene la función de eliminar el aire que se genera entre la piel del área a examinar y el transductor o sonda de ecógrafo, facilitando la transmisión de las ondas ultrasónicas.
2. Selección del tipo de transductor
Uno de los principales componentes del ecógrafo es el transductor o sonda. Existen diferentes tipos de transductores, cada uno está diseñado para explorar distintas regiones y profundidades. Mientras que los transductores lineales se emplean para estudios vasculares y superficiales, los modelos convexos son útiles para exploraciones abdominales profundas.
Por tanto, el profesional médico se encargará de selecciona el tipo de transductor adecuado, conectarlo al equipo y verificar su correcto funcionamiento antes de iniciar el estudio.
3. Emisión y recepción de ultrasonidos
Una vez preparado el transductor, el operador lo coloca sobre la zona cubierta con gel. El transductor emite ondas de ultrasonido de alta frecuencia que penetran en los tejidos internos del paciente. Cuando estas ondas atraviesan el cuerpo y se reflejan en las interfaces de los diferentes tejidos y órganos, las ondas reflejadas, denominadas ecos, regresan al transductor.
4. Captación de los ecos
El transductor actúa también como receptor, detectando las ondas reflejadas (ecos) que se generan desde las distintas estructuras internas. Estos ecos contienen información sobre la localización y las características de los tejidos atravesados, lo que permite analizar el estado y el funcionamiento de los diferentes órganos.
5. Procesamiento de la imagen
Los ecos captados por el transductor se convierten en señales eléctricas, que son procesadas por la consola del ecógrafo mediante diferentes algoritmos. El resultado es la generación de imágenes bidimensionales o tridimensionales en tiempo real que se visualizan en la pantalla del equipo.
Mediante el análisis de imágenes médicas, el operador puede observar la anatomía y el movimiento de los órganos y estructuras internas. A su vez, con el empleo del modo Doppler, se puede estudiar el flujo sanguíneo de los tejidos.
6. Exploración sistemática
El profesional realiza un barrido metódico moviendo el transductor sobre la zona de interés a analizar, obteniendo diferentes cortes (longitudinales, transversales, oblicuos) para examinar completamente los órganos y estructuras. Esta exploración sistemática es clave para obtener un diagnóstico completo y detallado, no omitir hallazgos relevantes y poder documentar adecuadamente los resultados.
7. Ajuste de parámetros de imagen
Durante la exploración, el operador puede ajustar diversos parámetros: desde la ganancia (brillo), la profundidad y el enfoque hasta el modo de visualización (2D, 3D, Doppler). De este modo, se podrá optimizar la calidad de imagen y adaptarla a las características anatómicas del paciente.
8. Interpretación de las imágenes médicas
Tras la realización de la exploración, el médico se encarga de analizar las imágenes obtenidas en tiempo real, identificar posibles alteraciones y realizar capturas estáticas o grabaciones de secuencias relevantes. Mediante estos registros, se podrá documentar de forma completa el informe final, que servirá de base para el diagnóstico y la toma de decisiones clínicas.
9. Finalización y limpieza
Al concluir el estudio, el operador retira el gel de la piel del paciente. Posteriormente, se debe seguir un protocolo de desinfección y limpieza del equipo utilizado, tanto el transductor como la superficie de contacto entre cada paciente.
Este proceso estructurado permite que la ecografía sea una técnica rápida, segura, no invasiva y muy versátil, facilitando la evaluación precisa de múltiples órganos y patologías en la práctica clínica diaria.
Principales aplicaciones clínicas del ecógrafo
El uso del ecógrafo abarca prácticamente todas las especialidades médicas. Entre las principales aplicaciones clínicas destacan las siguientes áreas:
Obstetricia y ginecología
La ecografía es fundamental en el seguimiento del embarazo, permitiendo evaluar el desarrollo fetal, la localización y viabilidad del embarazo, la detección de anomalías congénitas y el control de complicaciones obstétricas. También se utiliza para el estudio de patologías ginecológicas, como quistes ováricos, miomas uterinos o alteraciones endometriales.
Cardiología
El ecocardiograma es una técnica esencial para la valoración de la anatomía y función cardíaca, permitiendo diagnosticar enfermedades valvulares, miocardiopatías, insuficiencia cardíaca, cardiopatías congénitas y evaluar el flujo sanguíneo mediante el modo Doppler.
Medicina interna y gastroenterología
La ecografía abdominal permite examinar órganos como el hígado, la vesícula biliar, el páncreas, los riñones, el bazo y la vejiga. Por tanto, tiene un papel clave en el diagnóstico de masas, quistes, cálculos, inflamaciones y otras patologías. También se utiliza en la valoración de ascitis y en el control de procedimientos intervencionistas.
Exploración vascular
Mediante la ecografía Doppler, se evalúa el flujo sanguíneo en arterias y venas, por lo que se utiliza en el diagnóstico de trombosis venosa profunda, insuficiencia venosa, estenosis arteriales, aneurismas y otras enfermedades vasculares.
Músculo-esquelético
Permite estudiar músculos, tendones, ligamentos, articulaciones y partes blandas, facilitando el diagnóstico de lesiones deportivas, desgarros, tendinitis, bursitis, hemorragias y masas subcutáneas.
Urología
Se utiliza para valorar la próstata, la vejiga, los testículos y los riñones, siendo útil en el diagnóstico de hiperplasia prostática, litiasis, tumores y otras alteraciones urológicas.
Pediatría
La ecografía es especialmente útil en el estudio de patologías pediátricas, como la displasia de cadera, hidrocefalia, malformaciones renales y alteraciones abdominales en recién nacidos y lactantes.
Guía en procedimientos intervencionistas
El ecógrafo facilita la realización de biopsias, drenajes, punciones, colocación de catéteres y otras intervenciones, aumentando la seguridad y la precisión del procedimiento.
Medicina de urgencias y cuidado intensivos
Su rapidez y portabilidad permiten el diagnóstico inmediato de patologías graves como derrames pleurales, hemoperitoneo, neumotórax, taponamiento cardíaco y la evaluación rápida en pacientes politraumatizados (ecografía FAST).
Conclusión
El ecógrafo se ha consolidado como una herramienta esencial en la práctica clínica, ya que ofrece un análisis médico preciso, eficaz, seguro y en tiempo real sobre los diferentes órganos y tejidos internos. Su carácter no invasivo, la ausencia de radiación ionizante y su versatilidad para adaptarse a múltiples especialidades lo convierten en un recurso indispensable tanto en la evaluación inicial como en el seguimiento de numerosas patologías.
Su portabilidad y rapidez facilitan la toma de decisiones clínicas en distintos entornos, desde la consulta ambulatoria hasta situaciones de urgencia. Desde sus orígenes hasta la actualidad, el uso ecógrafo ha revolucionado la práctica médica, mejorando la calidad de la atención sanitaria y contribuyendo de manera decisiva a un diagnóstico temprano, preciso y seguro para los pacientes.
Si quieres obtener más información sobre ecógrafos u otro equipamiento de diagnóstico médico, puedes contactar con nosotros. Nuestro equipo de 4D te dará asesoramiento para buscar la mejor solución para tu clínica u hospital.
Contactar con 4D
Luís Daniel Fernández Pérez
Director de Diagximag. Distribuidor de soluciones y equipamiento médico de diagnóstico por imagen.